Что такое цитотоксический иммунитет
Что такое цитотоксический иммунитет
Цитотоксические аллергические реакции (гиперчувствительность II типа)
Аллергические реакции II типа могут носить системный или локализованный характер. Цитолитические реакции имеют место при переливании несовместимых групп крови, резус-несовместимости матери и плода, лежат в основе развития ряда аутоиммунных заболеваний, в частности, аутоиммунной лейкопении, анемии, тромбоцитопении, а также трансплантационного иммунитета и других форм патологии.
При аллергических реакциях II типа индуктором аллергии является антиген клеточной мембраны.
Возможны два основных варианта подобных антигенов:
1. Антиген является структурным компонентом клеточной мембраны (антигены гистосовместимости – МНС I и МНС II, Rh-антигены эритроцитов, антигены эритроцитов системы АВО и др.);
2. Органоспецифические антигены, модифицированные под влиянием ксенобиотиков, инфекционных патогенных факторов, воздействий физической или химической природы на структуру клеток.
Антигены, индуцирующие развитие цитолитических реакций, могут иметь и внеклеточное происхождение (антигены миелина, коллагена, базальной мембраны клубочков почек).
В отличие от анафилактических реакций при ряде цитотоксических реакций антиген-аллерген персистирует в организме, выполняя роль сенсибилизирующей и разрешающей доз воздействия, т.е. вызывает выработку антител-агрессоров и вступает с ними в реакции взаимодействия на клеточном уровне. Подобный феномен имеет место при аутоиммунных заболеваниях, трансплантационном иммунитете. В тех случаях, когда аллерген является естественным компонентом мембраны клеток (групповые или Rh-антигены эритроцитов) реакции развиваются при введении в организм комплементарных антител.
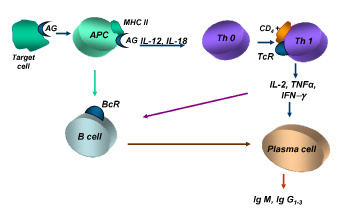
Антигенпрезентирующие клетки на фоне антигенной стимуляции обеспечивают не только экспрессию на цитоплазматических мембранах модифицированной части антигена в комплексе с белками гистосовместимости MHC II, но и интенсивную продукцию IL-12 и IL-18. Последние вызывают пролиферацию антигенчувствительного клона Th1. В свою очередь Th1 секретируют γ-интерферон, IL-2 и TNF-α, обеспечивающие переключение биосинтеза иммуноглобулинов в дифференцирующихся В-лимфоцитах с IgМ на IgG. Ответственными за развитие цитолитических реакций являются комплементсвязывающие цитолитические антитела классов IgG1, IgG2, IgG3 и IgM (рис. 1).
Рис. 1. Индукция иммунного ответа при цитотоксических реакциях
Различают три основных механизма цитолиза клеток в реакциях II типа:
• антителозависимая клеточная цитотоксичность;
• антителозависимый фагоцитоз опсонизированных клеток.
Комплементзависимый цитолиз обусловлен активацией комплемента комплексом антиген-антитело на мембране клеток по классическому пути, что приводит к формированию гидрофильного канала в мембране клетки с последующим развитием осмотического лизиса клетки.
Антителозависимая клеточная цитотоксичность возникает в том случае, если Fab-фрагменты аллергических антител связаны с антигеном клеточной мембраны, а к свободным Fc-фрагментам антител фиксируются макрофаги, эозинофилы, нейтрофилы с помощью соответствующих рецепторов. Нейтрофилы, макрофаги и NK-клетки обеспечивают цитолиз, взаимодействуя с Fc-фрагментом IgG, эозинофилы обеспечивают цитолиз при участии IgE и IgA.
В механизмах развития цитотоксичности при участии различных видов лейкоцитов важная роль отводится активации лизосомальных ферментов, освобождению катионных белков, лейкотриенов, лейкокининов, миелопероксидазы, свободных радикалов, вызывающих деструкцию клеток мишеней. Фагоцитоз опсонизированных клеток происходит в соответствии с общеизвестными закономерностями: разрушение клеток мишеней обеспечивается действием гидролитических ферментов в фаголизосомах, а также участием кислородзависимых и кислороднезависимых систем киллинга.
В последнее время выделяют четвертый механизм повреждающего действия на клетки-мишени, сопровождающийся развитием антителозависимой клеточной дисфункции (в ряде источников именуемые как рецепторно-опосредованные аллергические реакции, или V тип гиперчувствительности).
В роли антигенов при указанных реакциях выступают нейромедиаторы или гормоны (ацетилхолин, инсулин, тиреотропный гормон), индуцирующие синтез антител главным образом класса IgG.
Последние взаимодействуют со структурами, расположенными в рецепторном комплексе, вызывая стимулирующий или ингибирующий эффект на клетку-мишень.
Примером рецепторно-опосредованного стимулирующего типа аллергических реакций является развитие гипертиреоидного состояния при имитации антителами эффектов тиреотропного гормона. Описана возможность ингибирующего влияния антител на клетки и подавление ими эффектов инсулина.
Иммунокомплексные аллергические реакции (гиперчувствительность III типа)
Иммунокомплексная патология может носить локализованный и системный характер.
К местным проявлениям иммунокомплексной патологии относятся феномен Артюса, некоторые случаи лекарственной и пищевой аллергии. В ряде случаев иммунокомплексная патология приводит к развитию системных заболеваний (сывороточная болезнь, аутоиммунные заболевания, в частности гломерулонефрит, ревматоидный артрит, системная красная волчанка, артриты, эндокардит).
К числу аллергенов, вызывающих развитие иммунокомплексной патологии, относятся различные лекарственные препараты, антитоксические сыворотки, гамма-глобулины, пищевые, ингаляционные, вирусные и бактериальные аллергены.
К факторам риска развития иммунокомплексных реакций относится наследственная или приобретенная недостаточность системы элиминации иммунных комплексов, т.е. фагоцитоза, системы комплемента, недостаточность экспрессии CR1-рецепторов на мембранах эритроцитов, способных адсорбировать иммунные комплексы.
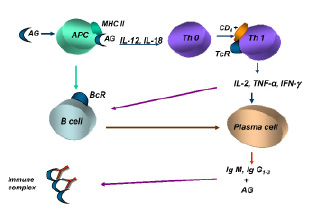
Механизмы развития иммунокомплексной патологии могут быть представлены следующим образом (рис. 2):
• презентация антигена макрофагами в комплексе с белками II класса МНС Тh1 и антигенчувствительным клонам В-лимфоцитов;
• секреция Тh1 гуморальных индукторов иммунопоэза ИЛ-2 и гамма-интерферона;
• стимуляция пролиферации и дифференцировки соответствующих антигенчувствительных клонов В-лимфоцитов, усиление продукции преципитирующих и комплементсвязывающих антител классов IgG1, IgG2, IgG3 и IgM.
Рис. 2. Индукция иммунного ответа при иммунокомплексных реакциях
При развитии иммунокомплексной патологии изначально ни антиген, ни антитело не связаны с клеточной мембраной. Образование высокотоксических растворимых комплексов происходит в системной циркуляции при условии взаимодействия антигена с антителом при небольшом избытке антигена; ММ токсических комплексов составляет 900`000 – 1`000`000. Они плохо фагоцитируются и долго находятся в организме.
Иммунные комплексы обладают способностью отслаивать эндотелий и фиксироваться на базальной мембране сосудов. При этом возникают обнажение коллагена, активация XII фактора Хагемана и связанного с ним каскада реакций освобождения медиаторов воспаления: активация калликреин-кининовой системы, коагуляционного и тромбоцитарного звеньев системы гемостаза, системы фибринолиза.
Для иммунокомплексных реакций характерно развитие выраженных расстройств микроциркуляции в различных органах и тканях, формирование циркуляторной гипоксии, снижение трофики органов и тканей, повышение проницаемости сосудистой стенки и другие нарушения.
Важная роль в патогенезе иммунокомплексной патологии отводится и медиаторам тучных клеток, тромбоцитов, нейтрофильных и базофильных лейкоцитов, активирующихся при участии антигена и системы комплемента.
Оценка показателей клеточного иммунитета
Первым исследованием всегда является подсчет лейкоцитарной формулы (см. главу «Гематологические исследования»). Оцениваются как относительные, так и абсолютные значения количества клеток периферической крови.
Определение основных популяций (Т-клетки, В-клетки, натуральные киллеры) и субпопуляций Т-лимфоцитов (Т-хелперы, Т-ЦТЛ). Для первичного исследования иммунного статуса и выявления выраженных нарушений иммунной системы ВОЗ рекомендовано определение CD3, CD4, CD8, CD19, CD16+56, соотношение CD4/CD8. Исследование позволяет определить относительное и абсолютное количество основных популяций лимфоцитов: Т-клетки – CD3, В-клетки – CD19, натуральные киллеры (NK) – CD3- CD16++56+, субпопуляции Т лимфоцитов (Т-хелперы CD3+ CD4+, Т-цитотоксические CD3+ CD8+ и их соотношение).
Иммунофенотипирование лимфоцитов проводится c использованием моноклональных антител к поверхностным дифференцировочным ангинам на клетках иммунной системы, методом проточной лазерной цитофлуорометрии на проточных цитофлуориметрах.
Выбор зоны анализа лимфоцитов производится по дополнительному маркеру CD45, который представлен на поверхности всех лейкоцитов.
Условия взятия и хранения образцов
Венозная кровь, взятая из локтевой вены, утром, строго натощак, в вакуумную систему до указанной на пробирке метки. В качестве антикоагулянта используется К2ЭДТА. После взятия пробирку с образцом медленно переворачивают 8-10 раз для перемешивония крови с антикоагулянтом. Хранение и транспортировка строго при 18–23°С в вертикальном положении не более 24 ч.
Невыполнение этих условий приводит к некорректным результатам.
Т-лимфоциты (CD3+ клетки). Повышенное количество свидетельствует о гиперактивности иммунитета, наблюдается при острых и хронических лимфолейкозах. Увеличение относительного показателя встречается при некоторых вырусных и бактериальных инфекциях в начале заболевания, обострениях хронических заболеваний.
Снижение абсолютного количества Т-лимфоцитов свидетельствует о недостаточности клеточного иммунитета, а именно о недостаточности клеточно-эффекторного звена иммунитета. Выявляется при воспалениях разнообразной этиологии, злокачественных новообразованиях, после травмы, операций, инфаркта, при курении, приеме цитостатиков. Повышение их числа в динамике заболевания – клинически благоприятный признак.
В-лимфоциты (CD19+ клетки) Снижение наблюдается при физиологических и врожденных гипогаммаглобулинемиях и агаммаглобулинемиях, при новообразованиях иммунной системы, лечении иммунодепрессантами, острой вирусной и хронической бактериальной инфекциях, состоянии после удаления селезенки.
Увеличение отмечается при аутоиммунных заболеваниях, хронических заболеваниях печени, циррозе, муковисцедозе, бронхиальной астме, паразитарных и грибковых инфекциях. Характерно в период реконвалесценции после перенесенных острых и хронических вирусных и бактериальных инфекций. Выраженное увеличение наблюдается при хроническом В-лимфолейкозе.
NK-лимфоциты с фенотипом CD3-CD16++56+ Натуральные киллеры (NK-клетки) – популяция больших гранулярных лимфоцитов. Они способны лизировать клетки-мишени, инфицированные вирусами и другими внутриклеточными антигенами, опухолевые клетки, а также другие клетки аллогенного и ксеногенного происхождения.
Увеличение количества NK-клеток связано с активацией антитрансплантационного иммунитета, в некоторых случаях отмечается при бронхиальной астме, встречается при вирусных заболеваниях, повышается при злокачественных новообразованиях и лейкозах, в периоде реконвалесценции.
Снижение наблюдается при врожденных иммунодефицитах, паразитарных инфекциях, аутоиммунных заболеваниях, облучении, лечении цитостатиками и кортикостероидами, стрессе, дефиците цинка.
Т-лимфоциты хелперы с фенотипом CD3+CD4+ Увеличение абсолютного и относительного количества наблюдается при аутоиммунных заболеваниях, может быть при аллергических реакциях, некоторых инфекционных заболеваниях. Это увеличение свидетельствует о стимуляции иммунной системы на антиген и служит подтверждением гиперреактивных синдромов.
Снижение абсолютного и относительного количества Т-клеток свидетельствует о гипореактивном синдроме с нарушением регуляторного звена иммунитета, является патогномичным признаком для ВИЧ-инфекции; встречается при хронических заболеваниях (бронхитах, пневмониях и т.д.), солидных опухолях.
Т-цитотоксические лимфоциты с фенотипом CD3+ CD8+ Повышение выявляется практически при всех хронических инфекциях, вирусных, бактериальных, протозойных инфекциях. Является характерным для ВИЧ-инфекции. Снижение наблюдается при вирусных гепатитах, герпесе, аутоиммунных заболеваниях.
Соотношение CD4+/CD8+ Исследование соотношения CD4+/CD8+ (CD3, CD4, CD8, CD4/CD8) рекомендовано только для мониторинга ВИЧ-инфекции и контроля эффективности АРВ терапии. Позволяет определить абсолютное и относительное количество Т-лимфоцитов, субпопуляций Т-хелперов, ЦТЛ и их соотношение.
Диапазон значений – 1,2–2,6. Снижение наблюдается при врожденных иммунодефицитах (синдром Ди-Джоржи, Незелофа, Вискотта-Олдрича), при вирусных и бактериальных инфекциях, хронических процессах, воздействии радиации и токсических химических веществ, множественной миеломе, стрессе, снижается с возрастом, при эндокринных заболеваниях, солидных опухолях. Является патогномичным признаком для ВИЧ-инфекции (менее 0,7).
Увеличение значения более 3 – при аутоиммунных заболеваниях, остром Т-лимфобластном лейкозе, тимоме, хроническом Т-лейкозе.
Изменение соотношения может быть связано с количеством хелперов и ЦТЛ у данного пациента. Например, снижение количества CD4+ Т-клеток при острой пневмонии в начале заболевания ведет к снижению индекса, а ЦТЛ при этом могут не измениться.
Для дополнительного исследования и выявления изменений иммунной системы при патологиях требующих оценки наличия острого или хронического воспалительного процесса и степени его активности, рекомендуется включать подсчет количества активированных Т-лимфоцитов с фенотипом CD3+HLA-DR+ и ТNK–клеток с фенотипом CD3+CD16++56+.
Т-активированные лимфоциты с фенотипом CD3+HLA-DR+ Маркер поздней активации, показатель гиперреактивности иммунитета. По экспрессии данного маркера можно судить о выраженности и силе иммунного ответа. Появляется на Т-лимфоцитах после 3-го дня острого заболевания. При благоприятном течении заболевания снижается до нормы. Увеличение экспрессии на Т-лимфоцитах может быть при многих заболеваниях, связанных с хроническим воспалением. Отмечено его повышение у пациентов с гепатитом С, пневмониями, ВИЧ-инфекцией, солидными опухолями, аутоиммунными заболеваниями.
ТNK-лимфоциты с фенотипом CD3+CD16++CD56+ Т-лимфоциты, несущие на своей поверхности маркеры CD16++ CD 56+. Эти клетки имеют свойства как Т-, так и NK-клеток. Исследование рекомендовано как дополнительный маркер при острых и хронических заболеваниях.
Снижение их в периферической крови может наблюдаться при различных органоспецифических заболеваниях и системных аутоиммунных процессах. Увеличение отмечено при воспалительных заболеваниях разной этиологии, опухолевых процессах.
Исследование ранних и поздних маркеров активации Т-лимфоцитов (CD3+CD25+, CD3-CD56+, CD95, CD8+CD38+) дополнительно назначают для оценки изменений ИС при острых и хронических заболеваниях, для диагностики, прогноза, мониторинга течения заболевания и проводимой терапии.
Т-активированные лимфоциты с фенотипом CD3+CD25+, рецeптор к ИЛ2 CD25+ – маркер ранней активации. О функциональном состоянии Т-лимфоцитов (CD3+) свидетельствует количество экспрессирующих рецепторов к ИЛ2 (CD25+). При гиперактивных синдромах количество этих клеток возрастает (острые и хронические лимфолейкозы, тимома, отторжение трансплантата), кроме того, повышение их может свидетельствовать о ранней стадии воспалительного процесса. В периферической крови их можно выявить в первые три дня болезни. Снижение числа этих клеток может наблюдаться при врожденных иммунодефицитах, аутоиммунных процессах, ВИЧ-инфекции, грибковых и бактериальных инфекциях, ионизирующей радиации, старении, отравлении тяжелыми металлами.
Т-цитотоксические лимфоциты с фенотипом CD8+CD38+ Присутствие CD38+ на ЦТЛ лимфоцитах отмечено у пациентов с разными заболеваниями. Информативный показатель при ВИЧ-инфекции, ожоговой болезни. Увеличение числа ЦТЛ с фенотипом CD8+CD38+ наблюдается при хронических воспалительных процессах, онкологических и некоторых эндокринных заболеваниях. При проведении терапии показатель снижается.
Субпопуляция натуральных киллеров с фенотипом CD3- CD56+ Молекула CD56 – адгезивная молекула, широко представленная в нервной ткани. Кроме натуральных киллеров, экспрессируется на многих типах клеток, в том число на Т-лимфоцитах.
Увеличение данного показателя свидетельствуют о расширении активности специфического клона клеток киллеров, которые имеют меньшую цитолитическую активность, чем NK-клетки с фенотипом CD3- CD16+. Количество этой популяции возрастает при гематологических опухолях (ЕК-клеточная или Т-клеточная лимфома, плазмоклеточная миелома, апластическая крупноклеточная лимфома), хронических заболеваниях, некоторых вырусных инфекциях.
Снижение отмечается при первичных иммунодефицитах, вирусных инфекциях, системных хронических заболеваниях, стрессе, лечении цитостатиками и кортикостероидами.
Рецептор CD95+ – один из рецепторов апоптоза. Апоптоз – сложный биологический процесс, необходимый для удаления из организма поврежденных, старых и инфицированных клеток. Рецептор CD95 экспрессируется на всех клетках иммунной системы. Он играет важную роль в контроле функционирования иммунной системы, так как является одним из рецепторов апоптоза. Его экспрессия на клетках определяет готовность клеток к апоптозу.
Снижение доли CD95+-лимфоцитов в крови пациентов свидетельствует о нарушении эффективности последнего этапа выбраковки дефектных и инфицированных собственных клеток, что может привести к рецидиву заболевания, хронизации патологического процесса, развитию аутоиммунных заболеваний и повышению вероятности опухолевой трансформации (к примеру, рака шейки матки при папилломотозной инфекции). Определение экспрессии CD95 имеет прогностическое значение при миело- и лимфопролифератиных заболеваниях.
Повышение интенсивности апоптоза наблюдается при вирусных заболеваниях, септических состояниях, при употреблении наркотических средств.
Активированные лимфоциты CD3+CDHLA-DR+, CD8+CD38+, CD3+CD25+, CD95. Тест отражает функциональное состояние Т-лимфоцитов и рекомендован для контроля за течением заболевания и контроля иммунотерапии при воспалительных заболеваниях разной этиологии.